流れ 2006年12月号 目次
― 特集: CFDを用いた流体機械最適設計の最前線 ―
| リンク一覧にもどる | |
多目的遺伝アルゴリズムの人工臓器設計・開発への応用
|
|
1. はじめに
厚生省の統計によると,現在の死亡原因のうち上位を占めるものは悪性 腫瘍 ,心疾患,脳血管疾患であるが,呼吸不全等の呼吸器疾患もこれらに迫る高死亡率な要因の一つとされている.今後, 環境要因の悪化や人口高齢化などにより,呼吸器疾患は益々増加する傾向にあり,それに伴い人工肺を用いた長期の呼吸補助などの適応症例も増加することが考えられ,安定したガス交換能,優れた抗血栓性,および十分な耐久性を有する人工肺の需要が高まっている.
現在,臨床使用されている人工肺のほとんどが,酸素ガスが中空糸の内側を,血液が中空糸の外側を流れる構造を持つ外部灌流型人工肺である.この人工肺は,血液が中空糸膜で構成される複雑な流路を流れることによって血流の高い攪拌効果が得られるため高いガス交換能,および低い圧力損失の利点を有する.しかし,その構造上,血液流動状態は,ハウジング形状,中空糸膜束形状,および流入出ポートの位置などの人工肺デザインに大きく依存し,ガス交換能,性抗血栓性など人工肺の性能に大きく影響を与える.
そこで本研究では,人工肺の設計・開発に多目的最適化問題を適用し,流体力学的見地から抗血栓性,および高ガス交換能を有する人工肺を,多目的遺伝アルゴリズム MOGA (Multi Objective Genetic Algorithm) と CFD (Computational Fluid Dynamics) を応用した人工肺形状の最適化システムにより設計し,牛血液を用いた in vitro 実験によりガス交換能に関して検討を行ったので報告する [1] .
2. 最適化システム
最適化システムは, 3 次元ソリッドモデラ SolidWorks (SolidWorks) , Microsoft Excel (Microsoft) ,自動メッシュ生成ツール PRO-AM (CDAJ) ,汎用数値流体解析ソフトウェアパッケージ STAR-CD (CDAJ) ,および多目的関数対応最適設計支援ツール modeFRONTIER (ESTECO) から構成される.これら異なるソフトウェアパッケージは modeFRONTIER のマクロによって動作する.本システムは, Pentium 4 3.6GHz CPU ( Intel ),および 2.0GB の RAM を搭載したパーソナルコンピュータ PRECISION 370 ( Dell )上に構成した.またオペレーティングシステムには Windows XP Professional ( Microsoft )を用いた.
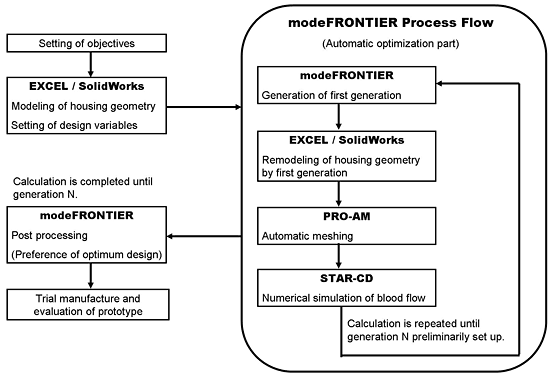
図 1 自動最適化システムのフローチャート
はじめに目的関数は,性能と関連性のある値の最大化,あるいは最小化など実験データに基づいた評価値が設定される.次に Excel/SolidWorks を用いて人工肺形状の作成,および設計変数の設定を行う.そして, modeFRONTIER を用いた MOGA による自動最適化のためのプロセスフローを作成する.本プロセスフローは, MOGA により初期世代を生成し, Excel/SolidWorks を用いて生成された初期世代による形状の変更を行い, PRO-AM により第一世代形状を自動でメッシュ生成し, STAR-CD により数値流体解析行う.数値流体解析の結果より MOGA が,目的関数に対する解の優越性を評価しながら次の世代を生成し,世代交代を繰り返すことにより,探索空間中の最適解を効率よく探索する.計算が予め設定しておいた世代数に達したら,パレート最適解より設計者が自分の価値観に見合った最適解を選好し,試作を行い in vitro ,または in vivo 実験にて評価を行う.また,初期世代の生成は,探索空間において一様に初期世代を生成することが可能な Sobol シーケンスを用いた.
3. 最適化
本最適化において目的関数は, 2 つ設定した.人工肺の中空糸膜部の血液流れにおいて 偏流・停滞などの淀みが生じた場合,膜面積を有効に利用することができずガス交換能が低下する.そのため,人工肺のガス交換能にとって中空糸膜へ均一に血液を流すことが重要である. そこで, 高ガス交換能を得るために 中空糸膜における流速の標準偏差の最小化 Min SD (Minimization of Standard Deviation) を目的関数として用いた. もう 1 つは抗血栓性に関するもので, 文献 [2] の血球の凝集する値を参考に流速 0.5mm/s の以下の領域の最小化 Min SA (Minimization of Stagnation Area) とした.
最適化のオリジナルデザインと設計変数を図 2 に示す.本人工肺の中空糸膜充填率は 25% ,膜面積は 0.68m2 とし ,血液充填量は 310ml であった.設計変数は,オリジナルデザインの流入出部において流入部断面高さ Hi1 , Hi2 , Hi3 , 流出部断面高さ Ho1 , Ho2 , Ho3 , 流入部断面間距離 Lbi , 流出部断面間距離 Lbo と 8 変数与えた.各設計変数の変位量と刻み幅は, Hi1 , Ho1 にて変位量 12 ~ 20mm ,刻み幅 2mm , Hi2 , Hi3 , Ho2 , Ho3 にて変位量 4 ~ 20mm ,刻み幅 2mm , Lbi , Lbo にて変位量: 5 ~ 90mm ,刻み幅: 5mm とした.
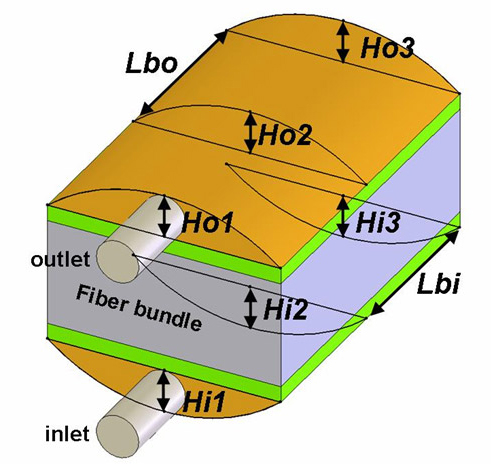
図 2 オリジナルデザインと設計変数
MOGA の計算は,初期世代数 32 個体,進化させる世代数 30 世代とし計 960 個体を用い,選択の適用確率 5% ,突然変異の適用確率 10% ,交叉の適用確率 50% として計算した. CFD 解析における支配方程式は Navier-Stokes の方程式,および連続の式を適用し, 有限体積法によって離散化し速度分布,圧力分布の数値解を得た. また,中空糸膜は多孔質媒体と見なし, Darcy の法則および Ergun の式を適用することで解析した. CFD 解析条件は,中空糸膜充填率 25% ,壁面滑りなし,流出部では自由流出を指定し,流入速度は 3L/min となる流速を与え,重力を流入部から流出部に 9.81m/s2 加えた.シミュレーション解析に用いた流体は非圧縮性ニュートン流体とし,粘性 3.3cP ,密度 1060kg/m3 の温度 37 ℃ における一般的な血液の特性条件を与えた.また,自動メッシュ生成による分割数は各形状において約 120,000 セルとし,メッシュの大きさは,中空糸膜部において 1 辺 1.5mm の 6 面体とした.
4. 結果
MOGA を用いた本自動最適化システムにより生成された形状の一例を図 3 に示す.右上の形状がオリジナルデザインで,左下の形状が 960 固体目の形状となっている.オリジナルデザインから形状が様々に変化し,流入出部において主に左右非対称の形状が MOGA によって生成された.本システムはおよそ 120 個体 / 日 の計算が可能であり, 960 固体の全計算はおよそ 8 日で完了した.

図 3 MOGA を用いた最適化により生成された人工肺形状
図 4 に最適化の結果として目的関数 Min SD と Min SA の散布図を示した. A 点がオリジナルデザインであり,それより優位な形状が多く生成された.本最適化における目的関数の関係は最小化 - 最小化であるので,破線がパレート最適解となり,パレート最適解上に 8 個体が存在した.パレート最適解は,その定義に基づいて modeFRONTIER が導出した.これらの個体から,設計者は自身の価値観により最適解を選好することができる.本最適化においては, Min SD に重点を置いた B 点を最適解 1 , Min SA に重点を置いた C 点を最適解 2 として選好した.最適解 1 をオリジナルデザインと比較すると Min SD において 75.1% , Min SA において 72.7% 改善した.最適解 2 をオリジナルデザインと比較すると Min SD において 61.7% , Min SA において 87.6% 改善した.以前の研究において手動にて最適化を行った形状が第 6 世代の固体( D 点)に存在した [3] .第 6 世代の固体のオリジナルデザインと比較した改善率は, Min SD において 29.7% , Min SA において 73.5% であった.
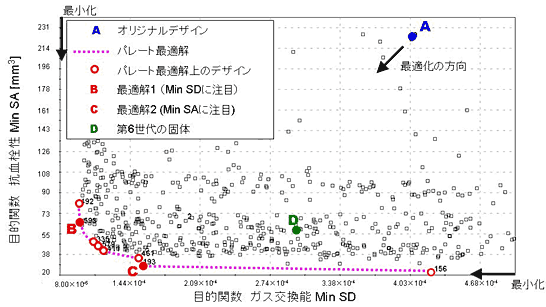
図 4 最適化結果の目的関数 Min SD と Min SA の散布図
CFD 解析結果の Min SD ,および Min SA を図 5 ,図 6 に示す. Min SD は,中空糸膜における流速の均一性を表す指標であるため,中空膜部の流速に重点を置いた速度分布を示す. 表示速度範囲の最大値を 18.1mm/s に,最低値を 6.5mm/s に変えた. Min SD は,その改善率が向上するに従い中空糸膜における偏流,および停滞の減少を確認できた.また, Min SD の改善率が最も高かった最適解 1 は,中空糸膜においてほぼ均一な速度分布を示した. Min SA として流速 0.5mm/s 以下の領域を流入部のものは水色,流出部のものは緑色で示した.流速 0.5mm/s 以下の領域 は, 主に流出部の辺縁部に観察され,オリジナルデザインと比較して最適解 1 ,最適解 2 ,第 6 世代の固体における流速 0.5mm/s 以下の領域は減少した.
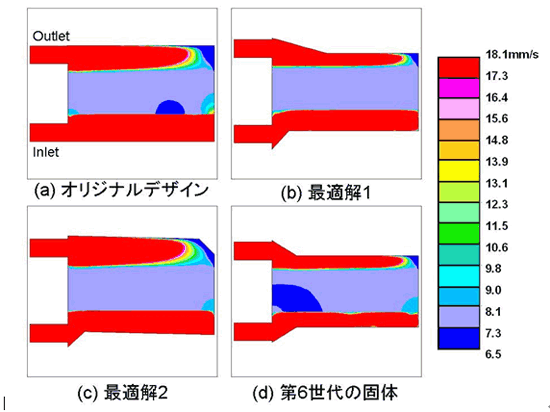
図 5 CFD 解析結果の Min SD
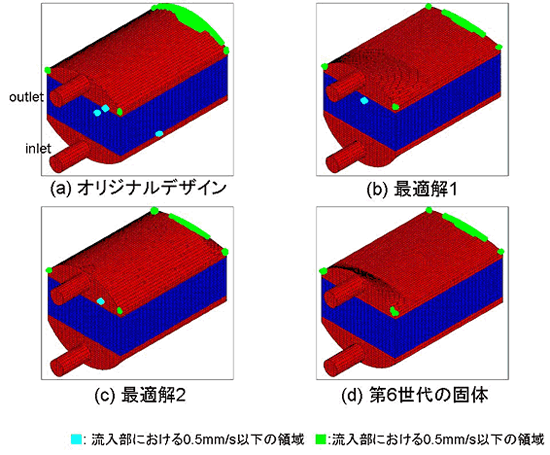
図 6 CFD 解析結果の Min SA
in vitro 評価実験結果には MOGA の有用性を検討するために,オリジナルデザイン,最適解 1 ,最適解 2 ,および進化の過程にある第 6 世代の固体を用いた.人工肺のハウジングの試作は,光造型によるマスターモデルからシリコン型をおこし, 真空注型装置 により シリコン型に ウレタン樹脂を注型して成型した.試作した人工肺を図 7 に示す.

図 7 試作した人工肺
in vitro 評価実験結果の酸素移動量を図 8 に,二酸化炭素移動量を図 9 に示す. Min SD の改善率が高くなるに従い,酸素移動量,および二酸化炭素移動量共に向上した.また最も高い改善率を示した最適解 1 における,酸素移動量はオリジナルデザインより平均で 18.4% 向上し,各流量において有意差が確認された.二酸化炭素移動量においては平均で 40.5% 向上し,血流量 2~5L の範囲で有意差が確認された.
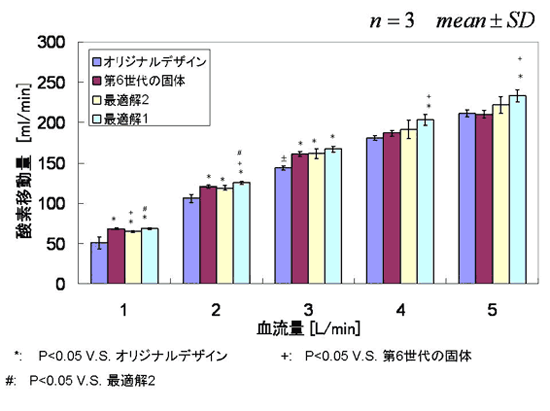
図 8 酸素移動量
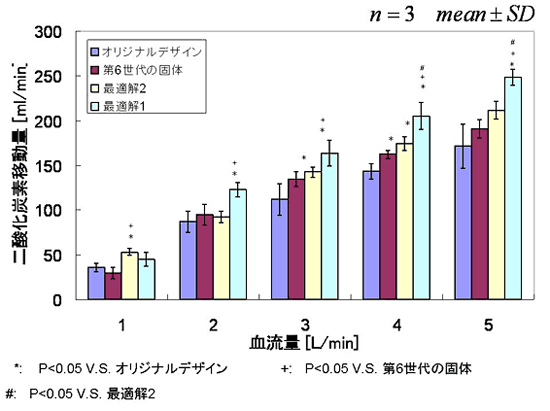
図 9 二酸化炭素移動量
5. まとめ
MOGA と CFD を応用した最適化システム は,長期使用などを目的とする次世代型の人工臓器の設計・開発における時間,コスト,労力を削減するだけでなく,人工臓器の高性能化への設計・開発支援システムとしての有効性が示唆された.
参考文献
[1] Taga I, Funakubo A and Fukui Y: Design and Development of an Artificial Implantable Lung using Multi Objective Genetic Algorithm (MOGA): Evaluation of Gas Exchange Performance: ASAIO J 51, 92-102, (2005).
[2] 舟久保昭夫,福井康裕:赤血球可視化による血液の流れの解析と血栓形成の検討 . 医用電子と生体工学 1992(30),46-53.2.
[3] Sato H, Taga I, Kinoshita T, Funakubo A, Ichiba S, Shimizu N: In vitro evaluation of a newly developed implantable artificial lung. Acta Med Okayama 60(2), 113-9, (2006)


